在老龄化趋势日益凸显的背景下,眼科领域作为增长潜力巨大的市场备受瞩目,国内外创新药企纷纷加快布局步伐。
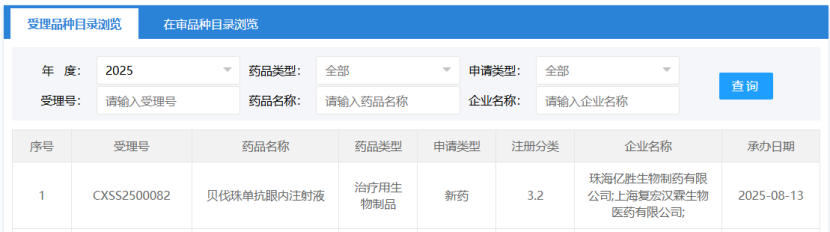
8月13日,CDE官网显示,复宏汉霖和亿胜生物共同开发的贝伐珠单抗眼内注射液(HLX04-O)申报上市。
据悉,HLX04-O是一款重组抗血管内皮生长因子(VEGF)人源化单抗,它能够特异性结合VEGF,阻断 VEGF 与内皮细胞上的受体 Flt1(VEGFR-1)和 KDR(VEGFR-2)结合,抑制其酪氨酸激酶信号通路的激活,进而抑制内皮细胞增生,减少新生血管生成,从而实现对湿性年龄相关性黄斑变性(wAMD)等血管增生眼部疾病的治疗。
市场普遍认为,作为重磅品种的摇篮,抗VEGF药物市场具有高速增长的潜力,吸引了越来越多的创新企业研发布局,尤其围绕长效、双靶点等差异化药物,跨国企业和本土企业皆在持续加速研发进程。
wAMD新药不断涌现
wAMD是50岁以上人口视力丧失和失明的主要原因,目前随着中国老龄化社会进程加快,相关药物需求开始增多。
2020年10月,亿胜生物与复宏汉霖达成全球许可协议,获得HLX04-O就眼科适应症的共同开发权益。今年4月,复宏汉霖宣布HLX04-O治疗wAMD中国患者的Ⅲ期HLX04-O-wAMD-CN研究已成功达到预设的主要研究终点。
研究结果显示,HLX04-O组第48周BCVA较基线改善的平均字母数变化结果非劣于雷珠单抗组,达到主要研究终点。此外,HLX04-O和雷珠单抗对wAMD患者人群整体、眼部、非眼部的安全性特征均相似,且安全性良好。
值得注意的是,HLX04-O不仅是国内第二个申报上市的贝伐珠单抗眼科制剂,也是第二个报产的针对wAMD的贝伐珠单抗。2个月前(6月12日),兆科眼科和东曜药业联合提交了3.2类新药贝伐珠单抗眼内注射溶液(TAB014)的上市申请。
随着亿胜生物与复宏汉霖入局,百亿眼科赛道的竞争愈发激烈。据了解,除了HLX04-O、TAB014两款尚在申请中的药物。6月24日,百奥泰宣布抗VEGF人源化单抗BAT5906针对wAMD的关键注册Ⅲ期临床研究成功达到预设的主要研究终点。百奥泰正在着手准备BAT5906的上市申请工作。
目前,国内已获批用于治疗wAMD的药物包括:诺华/罗氏开发的雷珠单抗(Ranibizumab)、诺华布西珠单抗(Brolucizumab),以及康弘药业的康柏西普(Conbercept)。其中,康柏西普结构上为100%人源化,能有效地结合VEGF-A、VEGF-B、PLGF等多个病理性新生血管相关的靶点。
此外,抗VEGF重组融合蛋白药Eylea(阿柏西普)由再生元和拜耳合作开发,5月22日,国家药监局批准艾力雅8mg(阿柏西普8mg,14.3mg/ml阿柏西普眼内注射溶液)用于治疗wAMD。
业内人士表示,贝伐珠单抗最初研发是应用于抗肿瘤领域,如今已成为多种实体瘤(如结直肠癌、肺癌、卵巢癌)的关键用药。其抗血管生成特性恰好契合wAMD等眼底病的病理机制,展现出“一药多靶”的特性潜力。
VEGF成眼科“新贵”
近年来,随着人口老龄化进程加快、生活方式变化、电子产品的普及等,眼部疾病的发病率及用药需求均在不断提升。
米内网数据显示,2023年中国公立医疗机构终端眼科用药(化学药+生物药)销售额超过140亿元,同比增长约18%。其中,康柏西普眼用注射液、雷珠单抗注射液、阿柏西普眼内注射液3款生物药位列2023年眼科用药前三,且销售额均超过10亿元。
其中,VEGF作为一类在细胞生长、血管生成和血管通透性调节中发挥关键作用的蛋白质家族,其异常表达也与多种眼科病变有关。除了wAMD,抗VEGF药物也在治疗糖尿病性黄斑水肿(DME)和视网膜静脉阻塞(RVO)等疾病上展示出良好效果。
优异的临床表现和潜在的蓝海市场,迎来了众多企业的入局。齐鲁制药是抗VEGF药物领域不可忽视的强者。2019年,齐鲁制药安可达获批上市,是国内首个获批的贝伐珠单抗生物类似药;2023年12月,齐鲁制药研发的阿柏西普生物类似药上市。2024年8月,齐鲁制药的雷珠单抗注射液获批上市,成为国内首个获批的雷珠单抗生物类似药,使其再次获得强效砝码。
今年5月,诺华宣布,其抗VEGF单抗倍优适(布西珠单抗)获批上市,用于治疗糖尿病黄斑水肿(DME)。此外,布西珠单抗治疗wAMD、增殖性糖尿病视网膜病变(PDR)适应症的上市许可申请已分别于 2024 年 10 月、2024 年 12 月提交。
业内人士指出,抗VEGF药物正在凭借其靶点和机制不断“开疆扩土”的同时,相关药物研发也在不断迭代升级,更优异临床效果和机制的新药开始崭露头角。市场无不认为,谁能在VEGF靶点上开发出更具优势的药物,谁就能在这一场眼科制剂争夺战中夺得市场竞争胜利的关键筹码。
差异化疗法谁拔头筹?
回头来看,眼病用药从最初的眼内注射到延长治疗间隔、到剂量升级,相关新药迭代在长效制剂上下足了功夫,不断提高患者依从性。
紧随其后,在多靶点研究上,已有新药崭露头角。例如,罗氏靶向VEGF-A和血管生成素-2(Ang-2)的法瑞西单抗问世,让患者获得了更优效药物同时,还让其仅用3年时间,便在2024年创造了44亿美元的年销售额。
在此前提下,罗氏乘胜追击,其基于DutaFab技术平台推进了下一代Ang2/VEGF-A双抗zifibancimig,通过兼容港式给药系统(PDS)的设计尝试将治疗间隔延长至每6个月1次。
国内方面,很多药企也敏锐捕捉到Ang2/VEGF-A双靶点的潜在机遇,正加速推进相关布局。目前,已有数款Ang2/VEGF双抗进入临床阶段,包括友芝友/康哲Y400(I/II期)、奥赛康/蔼睦医疗ASKG712(I期)、信达生物IBI-324(I期)、星眸生物XMVA09(II期)等。
值得注意的是,信达生物则是眼科赛道双靶点研发的强者,其抗VEGF+补体双靶点药物IBI302已进入Ⅲ期临床,VEGF-C/VEGF-A双抗IBI333的相关研究也在推进中。荣昌生物VEGF/FGF双靶点融合蛋白RC28-E也在Ⅲ期临床中。
此外,辉大生物则通过基因编辑手段,借助HG202辉大基因原创HG-PRECISE技术平台,将CRISPR/Cas13 RNA编辑器搭载于单个腺相关病毒(AAV)递送到视网膜,特异性地敲低VEGF-A mRNA表达水平,以治疗已接受过现有抗VEGF疗法有效或耐药的wAMD患者。
显然,随着眼科用药市场潜力不断兑现,国内眼科制剂市场也已进入进口+国产混战局面。业内人士指出,目前眼科赛道仍有巨大潜力未挖掘,Frost&Sullivan曾预测,中国眼科药物市场规模预计2025年将达到440亿元,2030年将达到1166亿元。未来,能在延长药物作用时间,减少药物注射次数,提高患者治疗依从性等方面做出差异化的企业,才能在该领域脱颖而出。
编辑:陈丽娜、张洁莹
版式编辑:于成林
审校:马飞、张松





还没有评论,来说两句吧...